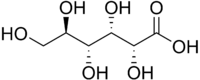
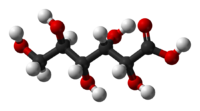
| Acido gluconico | |
|---|---|
 | |
 | |
| Nomi alternativi | |
| acido 2,3,4,5,6-pentaidrossiesanoico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H12O7 |
| Massa molecolare (u) | 196,16 |
| Aspetto | cristalli incolore |
| Numero CAS | |
| Numero EINECS | 208-401-4 |
| PubChem | 10690 |
| DrugBank | DB13180 |
| SMILES | C(C(C(C(C(C(=O)O)O)O)O)O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,24 |
| Temperatura di fusione | 131 °C (404,15 K) |
| Temperatura di ebollizione | 417 °C (690,15 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 314 |
| Consigli P | 280 - 305+351+338 - 310 [1] |
L'acido gluconico è un composto organico con formula bruta C6H12O7 e formula molecolare HOCH2(CHOH)4COOH. In soluzione acquosa a pH neutro, l'acido carbossilico è presente in forma dissociata, determinando lo ione gluconato; i corrispettivi sali sono chiamati gluconati. L'acido gluconico e i gluconati sono molto presenti in natura poiché questi composti hanno origine dall'ossidazione del glucosio.