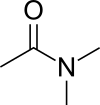
| Dimetilacetamid | |||
|---|---|---|---|
| |||

| |||
| IUPAC ime |
| ||
| Identifikacija | |||
| Abrevijacija | DMAc[2] | ||
| CAS registarski broj | 127-19-5 | ||
| PubChem[3][4] | 31374 | ||
| ChemSpider[5] | 29107 | ||
| UNII | JCV5VDB3HY | ||
| EINECS broj | |||
| MeSH | |||
| ChEMBL[6] | CHEMBL11873 | ||
| RTECS registarski broj toksičnosti | AB7700000 | ||
| Bajlštajn | 1737614 | ||
| Jmol-3D slike | Slika 1 Slika 2 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C4H9NO | ||
| Molarna masa | 87.12 g mol−1 | ||
| Agregatno stanje | Bezbona tečnost | ||
| Miris | Amoniacal | ||
| Gustina | 937 mg mL−1 | ||
| Tačka topljenja |
-20 °C, 253 K, -4 °F | ||
| Tačka ključanja |
165 °C, 438.2 K, 329 °F | ||
| Rastvorljivost u vodi | Meša se | ||
| log P | −0,253 | ||
| Napon pare | 300 Pa | ||
| λmax | 270 nm | ||
| Apsorbancija | 1,00 | ||
| Indeks prelamanja (nD) | 1,4375 | ||
| Viskoznost | 1,956 mPa s | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH |
−300,1 kJ mol−1 | ||
| Std entalpija sagorevanja ΔcH |
−2,5835–−2.5805 MJ mol−1 | ||
| Specifični toplotni kapacitet, C | 178,2 J K−1 mol−1 | ||
| Opasnost | |||
| EU-klasifikacija | |||
| EU-indeks | 616-011-00-4 | ||
| NFPA 704 | |||
| R-oznake | R61, R20/21 | ||
| S-oznake | S45 | ||
| Tačka paljenja | 63 °C | ||
| Tačka spontanog paljenja | 490 °C | ||
| Eksplozivni limiti | 1,8–11,5% | ||
| LD50 |
| ||
| Srodna jedinjenja | |||
| Srodna jedinjenja | |||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Dimetilacetamid (DMA) je organsko jedinjenje sa formulom CH3C(O)N(CH3)2. Ovo bezbojno jedinjenje se meša sa vodom. Ono ima visoku tačku ključanja. Koristi se kao polarni rastvarač u organskoj sintezi. DMA se meša sa većinom drugih rastvarača, mada je slabo rastvoran u alifatičnim ugljovodonicima.
