| 2C-B | |
|---|---|
 |
|
| Tunnisteet | |
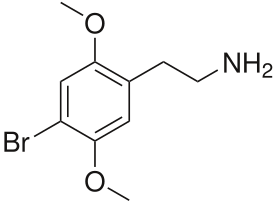
| IUPAC-nimi | 2-(4-bromi-2,5-dimetoksifenyyli)etanamiini |
| CAS-numero | |
| PubChem CID | |
| Ominaisuudet | |
| Molekyylikaava | C10H14NBrO2 |
| Moolimassa | 260.13 g g/mol |
2C-B eli 2,5-dimetoksi-4-bromifenetyyliamiini on psykedeeli, joka kuuluu 2C-kemikaalien ryhmään.[1] Ihmisissä se toimii päihteenä sitoutumalla osittaisagonistina 5-HT2A-serotoniinireseptoriin.[2] 2C-B luokiteltu laittomaksi huumeeksi monissa maissa.[3] 2C-B tunnetaan muun muassa myös nimillä BDMPEA, MFT ja α-desmetyyli-DOB (katso DOB).[4]
Kemialliset ominaisuudet
[muokkaa | muokkaa wikitekstiä]
2C-B:n hydrokloridi (2C-B-HCl) on kiteinen jauhe, joka voi olla valkoista tai heikon vaaleanpunaista. 2C-B-HCl:n CAS-numero on 56281-37-9. Se on liukoinen veteen,[4] etanoliin, DMSO:hon ja dimetyyliformamidiin.[5]
Päihdekäyttö
[muokkaa | muokkaa wikitekstiä]
Päihteenä 2C-B:tä käytetään yleensä suun kautta jauheen tai tablettien muodossa. Vaikutusten voimakkuuden kannalta 5–10 milligramman (mg) nieltyä annosta voidaan pitää heikkona, 10–25 mg annosta kohtalaisena ja 24–40 mg annosta vahvana.[1] Erowid-sivuston mukaan 2C-B:n vaikutukset ovat vahvimmat 45–75 minuutin kuluttua annoksen nielemisestä ja vaikutukset kestävät 4–6 tuntia.[6] Jotkin 2C-B:n käyttäjät käyttävät myös sitä nuuskaamalla.[7]
2C-B:n vaikutukset ovat psykedeeleille tyypillisiä. Se aiheuttaa esimerkiksi tunto-, näkö- ja kuuloaistin kautta välittyviä hallusinaatioita ja tunnetilan muutoksia, kuten euforiaa, hermostuneisuutta, ahdistusta tai sekavuutta. Se nostaa syketiheyttä ja verenpainetta hieman vaikutustensa ajaksi.[1] Se myös laajentaa pupilleja. Suuret 2C-B-annokset ovat hallusinogeenisiä, mutta pienet 2C-B-annokset voivat aiheuttaa jossain määrin MDMA:n kaltaisia vaikutuksia.[8] 2C-B ei kuitenkaan ole yhtä selkeästi empatogeeninen aine kuin MDMA.[9]
Ainakaan vuoteen 2018 mennessä yhtäkään 2C-B-yliannostuksen aiheuttamaa kuolemaa ei tiedetty tapahtuneen.[1] Yksi tapaus tunnetaan, jossa kooltaan tuntematon 2C-B-annos aiheutti serotoniinioireyhtymän, epilepsiaa ja aivoturvotusta.[8] Lisäksi tunnetaan ainakin kaksi tapausta, joista toisessa 2C-B:n käytön jälkeen ilmeni psykoosi ja toisessa aivojen verisuoniston vaskulopatia, mutta kummassakaan tapauksessa ei joko varmennettu 2C-B:n käyttöä potilailta otetuista näytteistä tai voitu sulkea pois sitä, että muut aineet olisivat aiheuttaneet nämä terveysongelmat.[10]
Toimintamekanismi
[muokkaa | muokkaa wikitekstiä]Ihmisissä 2C-B on ensisijaisesti 5-HT2A-serotoniinireseptorien osittaisagonisti. Tästä johtuvat sen psykedeeliset vaikutukset. Sen affiniteetti (Ki) tälle reseptorille on 6.9–8.6 nanomoolia per litra (nM) ja sen EC50 on 2.1–80 nM. Vertailun vuoksi LSD:n Ki on 3–5.3 nM ja EC50 44–260 nM samalle reseptorille. 2C-B sitoutuu myös ihmisten 5-HT1A-, 5-HT2B- ja 5-HT2C-serotoniinireseptoreihin agonistina, mutta heikommin. Sen affiniteetti näille on vastaavasti 240–311, 75–130 ja 43–47 nM.[11][2]
Ihmissä 2C-B on myös hyvin heikko norepinefriinitransportterien (NET), dopamiinitransportterien (DAT) ja serotoniinitransportterien (SERT) estäjä. 2-CB on lisäksi heikko dopamiinireseptorien, H1-histamiinireseptorin ja α1A- sekä α2A-adrenergisten reseptorien agonisti.[11]
Metabolia
[muokkaa | muokkaa wikitekstiä]Ihmisissä 2C-B:n aminoryhmä hapettuu aldehydiksi monoamiinioksidaasien vaikutuksesta. Aldehydeistä osa hapettuu aldehydidehydrogenaasilla karboksyylihapoksi tuottaen 4-bromi-2,5-dimetoksifenyylietikkahappoa (2C-B-CBA). Osa aldehydeistä taas pelkistyy alkoholidehydrogenaasilla alkoholiksi tuottaen 2-bromi-2,5-dimetoksifenyylietyylialkoholin (2C-B-ALC). 2C-B-CBA:n ja 2C-B-ALC:n OH-ryhmä voi glukuronidoitua. Myös muita aineenvaihduntatuotteita voi muodostua ja osa niistä muodostuu P450-entsyymien kautta.[3][12] Ihmisissä 2C-B-CBA on ollut pääasiallinen virtsaan poistuva aineenvaihduntatuote kun 2C-B:tä on käytetty suun kautta. Pieni osa 2C-B:stä poistuu virtsaan sellaisenaan ja muina aineenvaihduntatuotteina.[3]
Historia
[muokkaa | muokkaa wikitekstiä]Alexander Shulgin syntetisoi 2C-B:n ensimmäisenä vuonna 1974, jolloin hän myös havaitsi sen psykedeeliset vaikutukset koehenkilöissä.[13][3] 2C-B:tä havaittiin käytettävän laajemmin päihteenä ensi kerran vuonna 1985 USA:ssa.[14][3] Sitä myytiin 1980- ja 1990-luvuilla muun muassa nimillä Nexus, Erox, Performax, Toonies, Bromo, Spectrum ja Venus laillisena korvikkeena USA:ssa tuolloin hiljattain kielletylle MDMA:lle.[9] 2C-B puolestaan kiellettiin USA:ssa vuonna 1995.[9]
Euroopassa 2C-B:n käyttö yleistyi 1990-luvulla.[3] Esimerkiksi Alankomaissa sitä havaittiin käytettävän ensi kerran vuonna 1995, josta alkaen sitä ruvettiin myymään laillisesti ja avoimesti, kunnes se kiellettiin vuonna 1997.[15] Vuonna 2001 2C-B lisättiin YK:n vuoden 1971 psykotrooppisten aineiden luetteloon laittomaksi psykotrooppiseksi aineeksi.[1]
Vuoden 2015 arvion mukaan 2C-B:n käyttö oli ainakin tuolloin verrattain yleistä Euroopassa ja Australiassa suhteessa moniin muihin muuntohuumeisiin.[10]
Katso myös
[muokkaa | muokkaa wikitekstiä]- 2C-B-FLY
- NBOMe
- Psykedeeliset tryptamiinit
- Lysergihapon amidit
- Luettelo YK:n yleissopimusten mukaisista huumeista
Lähteet
[muokkaa | muokkaa wikitekstiä]- ↑ a b c d e E Papaseit et al: Acute pharmacological effects of 2C-B in humans: an observational study. Frontiers in Pharmacology, 2018, 9. vsk. PubMed:29593537. doi:10.3389/fphar.2018.00206. ISSN 1663-9812. Artikkelin verkkoversio.
- ↑ a b D Luethi et al: Monoamine receptor interaction profiles of 4-thio-substituted phenethylamines (2C-T drugs). Neuropharmacology, 2018, 134. vsk, nro Pt A, s. 141–148. PubMed:28720478. doi:10.1016/j.neuropharm.2017.07.012. ISSN 1873-7064. Artikkelin verkkoversio.
- ↑ a b c d e f T Kanamori et al: Analysis of 4-bromo-2,5-dimethoxyphenethylamine abuser's urine: identification and quantitation of urinary metabolites. Journal of Forensic Sciences, 2013, 58. vsk, nro 1, s. 279–287. PubMed:23066942. doi:10.1111/j.1556-4029.2012.02289.x. ISSN 1556-1057. Artikkelin verkkoversio.
- ↑ a b AC Moffat et al: Clarke's analysis of drugs and poisons: in pharmaceuticals, body fluids and postmortem material, s. 1056–1678. 4. painos. Pharmaceutical Press, 2011. ISBN 9780853697114.
- ↑ 2C-B (hydrochloride) caymanchem.com. Arkistoitu 12.11.2020. Viitattu 10.2.2020.
- ↑ Erowid 2C-B Vault: Basics www.erowid.org. Viitattu 9.2.2021.
- ↑ F Caudevilla-Gálligo et al: 4-Bromo-2,5-dimethoxyphenethylamine (2C-B): presence in the recreational drug market in Spain, pattern of use and subjective effects. Journal of Psychopharmacology, 2012, 26. vsk, nro 7, s. 1026–1035. PubMed:22234927. doi:10.1177/0269881111431752. ISSN 1461-7285. Artikkelin verkkoversio.
- ↑ a b AS Spoelder et al: Unexpected serotonin syndrome, epileptic seizures, and cerebral edema following 2,5‐dimethoxy‐4‐bromophenethylamine ingestion. Journal of Forensic Sciences, 2019, 64. vsk, nro 6, s. 1950–1952. PubMed:31643086. doi:10.1111/1556-4029.14214. ISSN 0022-1198. Artikkelin verkkoversio.
- ↑ a b c BV Dean et al: 2C or Not 2C: phenethylamine designer drug review. Journal of Medical Toxicology, 2013, 9. vsk, nro 2, s. 172–178. PubMed:23494844. doi:10.1007/s13181-013-0295-x. ISSN 1556-9039. Artikkelin verkkoversio.
- ↑ a b D González, M Torrens, M Farré: Acute effects of the novel psychoactive drug 2C-B on emotions. BioMed Research International, 2015. PubMed:26543863. doi:10.1155/2015/643878. ISSN 2314-6133. Artikkelin verkkoversio.
- ↑ a b A Rickli et al: Receptor interaction profiles of novel N-2-methoxybenzyl (NBOMe) derivatives of 2,5-dimethoxy-substituted phenethylamines (2C drugs). Neuropharmacology, 2015, 99. vsk, s. 546–553. PubMed:26318099. doi:10.1016/j.neuropharm.2015.08.034. ISSN 1873-7064. Artikkelin verkkoversio.
- ↑ T Kanamori et al: Synthesis and analysis of glucuronic acid-conjugated metabolites of 4-bromo-2,5-dimethoxyphenethylamine. Journal of Forensic Sciences, 2017, 62. vsk, nro 2, s. 488–492. PubMed:27874182. doi:10.1111/1556-4029.13266. ISSN 1556-4029. Artikkelin verkkoversio.
- ↑ AT Sulgin, MF Carter: Centrally active phenethylamines. Psychopharmacology Communications, 1975, 1. vsk, nro 1, s. 93–98. doi:10.1.1.691.2063. Artikkelin verkkoversio.
- ↑ FA Ragan et al: 4-Bromo-2,5-dimethoxyphenethylamine: identification of a new street drug. Journal of Analytical Toxicology, 1985, 9. vsk, nro 2, s. 91–93. doi:10.1093/jat/9.2.91. ISSN 0146-4760. Artikkelin verkkoversio.
- ↑ D Boer et al: More data about the new psychoactive drug 2C-B. Journal of Analytical Toxicology, 1999, 23. vsk, nro 3, s. 227–228. PubMed:10369336. doi:10.1093/jat/23.3.227. ISSN 0146-4760. Artikkelin verkkoversio.
Aiheesta muualla
[muokkaa | muokkaa wikitekstiä]- 2C-B:n Erowid-portaali (englanniksi)
- PiHKAL-kirja osoitteessa Erowid (englanniksi)
- isomerdesign.com (englanniksi)
- PubChem: 2-(4-bromo-2,5-dimethoxyphenyl)ethylamine (englanniksi)
- DrugBank: 4-Bromo-2,5-dimethoxyphenethylamine (englanniksi)
- 2C-B:n ja muiden päihteiden synteesi (englanniksi)
| Amfetamiinit |
3C-E | 4-FMP | 4-MTA | Alfametyylidopamiini | Amfetamiini | Bentsfetamiini | Bromo-DragonFLY | Deksamfetamiini | Dimetoksiamfetamiini | DOB | DOC | DOI | DOM | Efedriini | Fenfluramiini | Katiini | Levoamfetamiini | Levometamfetamiini | Lisdeksamfetamiini | MBDB | MDA | MDE | MDMA | Metamfetamiini | PMA | Pseudoefedriini | Tranyylisypromiini |
|---|---|
| Katekoliamiinit | |
| Katinonit |
4-bromimetkatinoni | Bupropioni | Katinoni | Mefedroni | Metkatinoni | Dimetyylikatinoni |
| Muut |
2C-B | 2C-B-FLY | 2CBFly-NBOMe | 2C-C | 2C-D | 2C-E | 2C-F | 2C-I | 2C-N | 2C-SE | 2C-T | 2C-T-2 | 2C-T-4 | 2C-T-7 | 2C-T-8 | 2C-T-21 | 2C-TFM | 25C-NBOMe | 25I-NB34MD | 25I-NBF | 25I-NBMD | 25I-NBOMe | 25P-NBOMe | 25TFM-NBOMe | Allyylieskaliini | Eskaliini | Fenformiini | Fentermiini | HOT-7 | Meskaliini | Metyylifenidaatti | Synefriini | Trifluorimeskaliini | Tyramiini |