Si ce bandeau n'est plus pertinent, retirez-le. Cliquez ici pour en savoir plus.
La mise en forme de cet article est à améliorer (juillet 2024).
La mise en forme du texte ne suit pas les recommandations de Wikipédia : il faut le « wikifier ».
| Glucokinase | ||
 Glucokinase humaine (PDB 1V4S[1]) | ||
| Caractéristiques générales | ||
|---|---|---|
| Symbole | GCK | |
| N° EC | 2.7.1.2 | |
| Homo sapiens | ||
| Locus | 7p13 | |
| Masse moléculaire | 52 191 Da[2] | |
| Nombre de résidus | 465 acides aminés[2] | |
| Liens accessibles depuis GeneCards et HUGO. | ||
La glucokinase est une phosphotransférase qui catalyse la réaction :

|
+ ATP → ADP + H+ + | 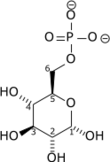
|
| Glucose | Glucose-6-phosphate |
La glucokinase bactérienne est spécifique au glucose (EC ), de même que celle des vertébrés, qui est une isoforme d'hexokinase (EC ), appelée de ce fait hexokinase D ou hexokinase type IV[3]. La glucokinase des mammifères est exprimée au niveau du foie et des cellules β des îlots de langerhans dans le pancréas.
Cette enzyme est caractérisée par :
- une faible affinité pour le glucose qui se traduit par une constante de semi-saturation beaucoup plus élevée (10 mM) que celles observées chez les trois autres isoenzymes ;
- une faible coopérativité positive avec le glucose (constante de Hill de 1,5), qu’on ne peut pas expliquer par les mécanismes classiques de coopérativité parce qu’il s’agit d’une enzyme monomérique avec un seul site de liaison au glucose. Dans la mesure où elle ne suit pas l’équation de Michaelis-Menten, on ne peut parler d’une constante de Michaelis ;
- l’absence totale d’inhibition par le glucose-6-phosphate, son produit, aux concentrations physiologiques, ce qui est une grande différence avec les autres trois isoenzymes (hexokinases A, B et C).
La « glucokinase » répond bien au besoin du foie qui doit faire face aux afflux importants de glucose en période post-prandiale afin de le stocker sous forme de glycogène.
Glucokinase
| N° EC | EC |
|---|---|
| N° CAS |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
Notes et références
[modifier | modifier le code]- (en) Kenji Kamata, Morihiro Mitsuya, Teruyuki Nishimura, Jun-ichi Eiki et Yasufumi Nagata, « Structural Basis for Allosteric Regulation of the Monomeric Allosteric Enzyme Human Glucokinase », Structure, vol. 12, no 3, , p. 429-438 (PMID 15016359, DOI 10.1016/j.str.2004.02.005, lire en ligne)
- Les valeurs de la masse et du nombre de résidus indiquées ici sont celles du précurseur protéique issu de la traduction du gène, avant modifications post-traductionnelles, et peuvent différer significativement des valeurs correspondantes pour la protéine fonctionnelle.
- (en) Cárdenas M.L., Cornish-Bowden A., Ureta T., « Evolution and regulatory role of the hexokinases », Biochim. Biophys. Acta, vol. 1401, , p. 242–264 (PMID 9540816)
- (en) Vladimir V. Lunin, Yunge Li, Joseph D. Schrag, Pietro Iannuzzi, Miroslaw Cygler et Allan Matte, « Crystal Structures of Escherichia coli ATP-Dependent Glucokinase and Its Complex with Glucose », Journal of Bacteriology, vol. 186, no 20, , p. 6915-6927 (PMID 15466045, PMCID 522197, DOI 10.1128/JB.186.20.6915-6927.2004, lire en ligne)
Voir aussi
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- Glucokinase and Glycemic Disease: from Basics to Novel Therapeutics (ed. F. M. Matschinsky & M. A. Magnuson), Karger, Bâle, Suisse, 2004.
- M. L. Cárdenas (1995) “Glucokinase”: its regulation and role in liver metabolism, R. G. Landes Co, Austin, USA.
