| ADN metiltransferase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
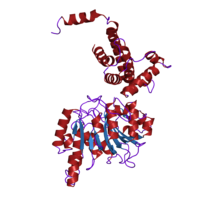 estrutura cristalina do encima de restrición de tipo I proteína ecoki m (ec 2.1.1.72) (m.ecoki) | |||||||||
| Identificadores | |||||||||
| Símbolo | N6_Mtase | ||||||||
| Pfam | PF02384 | ||||||||
| Pfam clan | CL0063 | ||||||||
| InterPro | IPR003356 | ||||||||
| PROSITE | PDOC00087 | ||||||||
| |||||||||
| ADN metiltransferase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | HsdM_N | ||||||||
| Pfam | PF12161 | ||||||||
| |||||||||
| ADN metiltransferase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
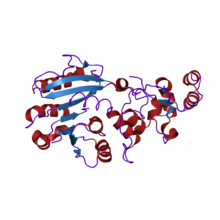 estrutura da dnmt2 humana, un homólogo enigmático de ADN metiltransferas | |||||||||
| Identificadores | |||||||||
| Símbolo | DNA_methylase | ||||||||
| Pfam | PF00145 | ||||||||
| Pfam clan | CL0063 | ||||||||
| InterPro | IPR001525 | ||||||||
| PROSITE | PDOC00089 | ||||||||
| SCOPe | 1hmy / SUPFAM | ||||||||
| CDD | cd00315 | ||||||||
| |||||||||
| ADN metiltransferase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
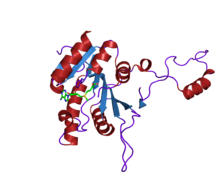 estrutura cristalina da metiltransferase mboiia (Moraxella bovis) | |||||||||
| Identificadores | |||||||||
| Símbolo | N6_N4_Mtase | ||||||||
| Pfam | PF01555 | ||||||||
| Pfam clan | CL0063 | ||||||||
| InterPro | IPR002941 | ||||||||
| PROSITE | PDOC00088 | ||||||||
| SCOPe | 1boo / SUPFAM | ||||||||
| |||||||||
En bioquímica, a familia da ADN metiltransferase (ou DNA metiltransferase, DNA MTase) é unha familia de encimas que cataliza a transferencia dun grupo metilo (CH3) ao ADN. A metilación do ADN é necesaria para moitas funcións biolóxicas. Todas as ADN metiltransferases usan a S-adenosilmetionina (SAM) como doante de metilos.
Clasificación
[editar | editar a fonte]Substrato
[editar | editar a fonte]As MTases poden dividirse en tres tipos segundo as reaccións químicas que catalizan:
- m6A - que xeran N6-metiladenina EC 2.1.1.72
- m4C - que xeran N4-metilcitosina EC 2.1.1.113
- m5C - que xeran C5-metilcitosina EC 2.1.1.37
As m6A e m4C metiltransferases encóntranse fundamentalmente en procariotas. As m5C metiltransfereases encóntranse nalgúns eucariotas inferiores, na maioría das plantas superiores e en moitos animais.
As m6A metiltransferases (ADN metilase específica de adenina N-6) (A-Mtase) son encimas que metilan especificamente o grupo amino en posición C-6 de adeninas no ADN. Atópanse nos tres tipos existentes de sistemas de restrición-modificación bacterianos (nos sistemas de tipo I a A-Mtase é o produto do xene hsdM, e nos de tipo III é o produto do xene mod). Estes encimas son responsables da metilaciónde secuencias específicas de ADN coa finalidade de impediren que o hóspede dixira o seu propio xenoma por medio dos seus propios encimas de restrición. Estas metilases teñen a mesma especificidade de secuencia que os seus encimas de restrición correspondentes. Estes encimas conteñen un motivo conservado, que é Asp/Asn-Pro-Pro-Tyr/Phe, situado nas súas seccións N-terminais. Esta rexión conservada podería estar implicada na unión co substrato ou na actividade catalítica.[1][2][3][4] Obtívose a estrutura secundaria da N6-MTase TaqI (M.TaqI) a unha resolución de 2,4 Å. A molécula está pregada formando dous dominios, un dominio N-terminal catalítico, que contén os sitios de unión catalíticos e para o cofactor, e comprende unha folla beta de 9 febras central, rodeada de 5 hélices; e un dominio de recoñecemento do ADN C-terminal, que está formado por 4 pequenas follas beta e 8 hélices alfa. Os dominios N- e C-terminais forman unha fenda que acomoda o substrato (ADN).[5] Propúxose unha clasificación das N-MTases, baseada nos arranxos dos motivos conservados (CM).[4] Segundo esta clasificación, as N6-MTases que teñen un motivo DPPY (CM II) que aparece despois do motivo FxGxG (CM I) denomínanse N6-adenina MTases de clase D12. O sistema de restrición-modificación está composto por tres polipéptidos, chamados R, M e S. As subunidades M (hsdM) e S xuntas forman unha metiltransferase que metila dous residuos de adenina en febras complementarias dunha secuencia de recoñecemento do ADN bipartita. En presenza da subunidade R, o complexo pode tamén actuar como unha endonuclease, uníndose á mesma secuencia diana pero cortando o ADN a certa distancia dese sitio. Que o ADN sexa cortado ou modificado depende do estado de metilación da secuencia diana. Cando o sitio diana non está modificado, o ADN vai ser cortado, pero cando o sitio diana está hemimetilado, o complexo actúa como unha metiltransferase de mantemento, modificando o ADN para que ambas as febras sexan metiladas. O hsdM contén un dominio en hélice alfa no N-terminal, chamado dominio HsdM N-terminal.[6]
As m4C metiltransferases (ADN metilases específicas de citosina N-4) son encimas que metilan especificamente o grupo amino na posición C-4 de citosinas no ADN.[4] Estes encimas son compoñentes dos sistemas de restrición modificación de tipo II de procariotas. Recoñecen unha secuencia específica no ADN e metilan unha citosina desa secuencia. Con esta acción protexen o ADN da clivaxe realizada polos encimas de restrición de tipo II que recoñecen a mesma secuencia.
As m5C metiltransferases (ADN metilases específicas de citosina C-5) (C5 Mtase) son encimas que metilan especificamente o carbono C-5 de citosinas no ADN para producir C5-metilcitosina.[7][8][9] En células de mamífero, as metiltransferases específicas de citosina metilan certas secuencias CpG, que se cre que modulan a expresión xénica e a diferenciación celular. En bacterias, estes encimas son un compoñente dos sistemas de restrición-modificación e serven como ferramentas valiosas para a manipulación do ADN.[8][10] A estrutura secundaria da metiltransferase HhaI (M.HhaI) obtívose cunha resolución de 2,5 Å: a molécula prégase en dous dominios, un máis grande e catalítico, que contén o sitio catalítico e o do cofactor, e outro máis pequeno para o recoñecmento do ADN.[11]
De novo e de mantemento
[editar | editar a fonte]As metiltransferases de novo recoñecen algún sinal no ADN que fai que metilen a máis (novas) citosinas. Estes encimas exprésanse principalmente nas etapa temperás do desenvolvemento embrionario e establecen o patrón de metilación.
As metiltransferases de mantemento metilan o ADN cando unha febra está xa metilada. Funcionan durante toda a vida do organismo para manteren o patrón de metilación que fora previamente establecido polas metiltransferases de novo.
Mamíferos
[editar | editar a fonte]Identificáronse tres ADN metiltransferases activas en mamíferos. Chámanse DNMT1,[12] DNMT3A,[13] e DNMT3B.[14] Un cuarto encima previamente coñecido como DNMT2 non é, en realidade, unha ADN metiltransferase (véxase máis abaixo).
A DNMT3L[15] é unha proteína moi relacionada con DNMT3A e DNMT3B en estrutura e fundamental para a metilación do ADN, pero parece que é inactiva por si soa.
DNMT1
[editar | editar a fonte]A DNMT1 é a ADN metiltransferase máis abondosa nas células de mamíferos, e considérase que é a metiltransferase de mantemento esencial en mamíferos. Metila predominantemente dinucleótidos CpG hemimetilados no xenoma de mamíferos. Este encima é de 7 a 100 veces máis activo no ADN hemimetilado en comparación co substrato non metilado in vitro, pero é aínda máis activo realizando a metilación de novo que outras DNMTs. O motivo de recoñecemento do encima humano implica só tres das bases no par dinucleotídico CpG: unha C nunha febra e CpG na outra. Este especificidade de substrato pouco estrita permítelle que metile estruturas infrecuentes como intermediarios de slippage no ADN a velocidades de metiltransferase de novo que igualan as súas velocidades como metiltransferase de mantemento.[16] Como outras ADN metiltransferases citosina-5, o encima humano recoñece certas citosinas en ADN bicatenario e funciona por medio dun ataque nucleofílico.[17] En células cancerosas humanas, a DNMT1 é responsable tanto da metilación de novo coma da de mantemento dos xenes supresores de tumores.[18][19] O encima ten uns 1.620 aminoácidos. Os seus primeiros 1.100 aminoácidos constitúen o dominio regulador do encima, e os restantes forman o dominio catalítico. Estes dominios están unidos por repeticións de Gly-Lys. Requírense os dous dominios para a función catalítica da DNMT1.
A DNMT1 ten varias isoformas, que son: a DNMT1 somática, unha variante de empalme (DNMT1b) e unha isoforma específica do ovocito (DNMT1o). A DNMT1o sintetízase e almacénase no citoplasma do ovocito e é translocada ao núcleo celular durante o desenvolvemento embrionario temperán, mentres que a DNMT1 somática encóntrase sempre no núcleo das células dos tecidos somáticos.
O mutante nulo para DNMT1 de células nai embrionarias é viable e contén unha pequena porcentaxe de ADN metilado e actividade de metiltransferase. Os embrións de rato homocigotos para unha deleción en Dnmt1 morren aos 10–11 días de xestación.[20]
TRDMT1
[editar | editar a fonte]Aínda que este encima ten fortes semellanzas de secuencia coas 5-metilcitosina metiltransferases de procariotas e de eucariotas, en 2006, atopouse que o encima metilaba a posición 38 nun ARN transferente do ácido aspártico e non metilaba o ADN.[21] Para reflectir na nomenclatura esta diferente función, o nome desta metiltransferase foi cambiado de DNMT2 a TRDMT1 (ARNt do ácido aspártico metiltransferase 1), que indica mellor a súa función biolóxica.[22] A TRDMT1 é a primeira ARN citosina metiltransferase que foi identificada en humanos.
DNMT 3
[editar | editar a fonte]A DNMT3 é unha familia de ADN metiltransferases que poden metilar á mesma velocidade sitios CpG hemimetilados e non metilados.[23] A arquitectura dos encimas DNMT3 é similar á dos DNMT1, xa que teñen unha rexiónn reguladora unida a a un dominio catalítico. Coñécense tres membros da familia DNMT3, que son: DNMT3a, 3b, e 3L.
A DNMT3a e a DNMT3b poden mediar a represión de xenes independente de metilación. A DNMT3a pode colocalizar xunto coa proteína da heterocromatina 1 (HP1) e a proteína de unión a metil CpG (MeCBP). Tamén poden interaccionar con DNMT1, o cal podería ser un evento cooperativo durante a metilación do ADN. A DNMT3a prefire a metilación de CpG mellor que a metilación de CpA, CpT, e CpC, aínda que parece ser que DNMT3a e DNMT3b teñen certa preferencia de secuencia de metilación. A DNMT3a metila sitios CpG a unha velocidade moito máis lenta que DNMT1, pero maior que a de DNMT3b.
A DNMT3L contén un motivo de ADN metiltransferase e é necesaria para establecer a impronta xenómica materna, a pesar de ser cataliticamente inactiva. A DNMT3L exprésase durante a gametoxénese cando ten lugar a impronta xenómica. A perda de DNMT3L dá lugar á expresión bialélica de xenes que normalmente non se expresan polo alelo materno. A DNMT3L interacciona con DNMT3a e DNMT3b e está colocalizada no núcleo. Aínda que a DNMT3L parece ser incapaz de metilar, pode participar na represión da transcrición.
Importancia clínica
[editar | editar a fonte]Debido aos efectos epixenéticos da familia DNMT, están a investigarse algúns inhibidores de DNMT para o tratamento dalgúns cancros. Entre eles están:[24]
- Vidaza (azacitidina) en ensaios en fase III para as síndromes mielodisplásticas e a leucemia mieloide aguda.
- Dacogen (decitabina) en ensaios en fase III para a leucemia mieloide aguda e a leucemia mielóxena crónica.
Notas
[editar | editar a fonte]- ↑ Loenen WA, Daniel AS, Braymer HD, Murray NE (November 1987). "Organization and sequence of the hsd genes of Escherichia coli K-12". J. Mol. Biol. 198 (2): 159–70. PMID 3323532. doi:10.1016/0022-2836(87)90303-2.
- ↑ Narva KE, Van Etten JL, Slatko BE, Benner JS (December 1988). "The amino acid sequence of the eukaryotic DNA [N6-adenine]methyltransferase, M.CviBIII, has regions of similarity with the prokaryotic isoschizomer M.TaqI and other DNA [N6-adenine] methyltransferases". Gene 74 (1): 253–9. PMID 3248728. doi:10.1016/0378-1119(88)90298-3.
- ↑ Lauster R (March 1989). "Evolution of type II DNA methyltransferases. A gene duplication model". J. Mol. Biol. 206 (2): 313–21. PMID 2541254. doi:10.1016/0022-2836(89)90481-6.
- ↑ 4,0 4,1 4,2 Timinskas A, Butkus V, Janulaitis A (May 1995). "Sequence motifs characteristic for DNA [cytosine-N4] and DNA [adenine-N6] methyltransferases. Classification of all DNA methyltransferases". Gene 157 (1–2): 3–11. PMID 7607512. doi:10.1016/0378-1119(94)00783-O.
- ↑ Labahn J, Granzin J, Schluckebier G, Robinson DP, Jack WE, Schildkraut I, Saenger W (November 1994). "Three-dimensional structure of the adenine-specific DNA methyltransferase M.Taq I in complex with the cofactor S-adenosylmethionine". Proc. Natl. Acad. Sci. U.S.A. 91 (23): 10957–61. PMC 45145. PMID 7971991. doi:10.1073/pnas.91.23.10957.
- ↑ Kelleher JE, Daniel AS, Murray NE (1991). "Mutations that confer de novo activity upon a maintenance methyltransferase". Journal of Molecular Biology 221 (2): 431–440. PMID 1833555. doi:10.1016/0022-2836(91)80064-2.
- ↑ Pósfai J, Bhagwat AS, Roberts RJ (December 1988). "Sequence motifs specific for cytosine methyltransferases". Gene 74 (1): 261–5. PMID 3248729. doi:10.1016/0378-1119(88)90299-5.
- ↑ 8,0 8,1 Kumar S, Cheng X, Klimasauskas S, Mi S, Posfai J, Roberts RJ, Wilson GG (January 1994). "The DNA (cytosine-5) methyltransferases". Nucleic Acids Res. 22 (1): 1–10. PMC 307737. PMID 8127644. doi:10.1093/nar/22.1.1.
- ↑ Lauster R, Trautner TA, Noyer-Weidner M (March 1989). "Cytosine-specific type II DNA methyltransferases. A conserved enzyme core with variable target-recognizing domains". J. Mol. Biol. 206 (2): 305–12. PMID 2716049. doi:10.1016/0022-2836(89)90480-4.
- ↑ Cheng X (February 1995). "DNA modification by methyltransferases". Curr. Opin. Struct. Biol. 5 (1): 4–10. PMID 7773746. doi:10.1016/0959-440X(95)80003-J.
- ↑ Cheng X, Kumar S, Posfai J, Pflugrath JW, Roberts RJ (July 1993). "Crystal structure of the HhaI DNA methyltransferase complexed with S-adenosyl-L-methionine". Cell 74 (2): 299–307. PMID 8343957. doi:10.1016/0092-8674(93)90421-L.
- ↑ "DNMT1". Gene Symbol Report. HUGO Gene Nomenclature Committee. Arquivado dende o orixinal o 06 de outubro de 2013. Consultado o 2012-09-27.
- ↑ "DNMT3A". Gene Symbol Report. HUGO Gene Nomenclature Committee. Arquivado dende o orixinal o 09 de setembro de 2013. Consultado o 2012-09-27.
- ↑ "DNMT3B". Gene Symbol Report. HUGO Gene Nomenclature Committee. Arquivado dende o orixinal o 21 de setembro de 2013. Consultado o 2012-09-27.
- ↑ "DNMT3L". Gene Symbol Report. HUGO Gene Nomenclature Committee. Arquivado dende o orixinal o 07 de outubro de 2013. Consultado o 2012-09-27.
- ↑ Kho MR, Baker DJ, Laayoun A, Smith SS (1998). "Stalling of Human DNA (Cytosine-5) Methyltransferase at Single Strand Conformers form a Site of Dynamic Mutation". Journal of Molecular Biology 275 (1): 67–79. PMID 9451440. doi:10.1006/jmbi.1997.1430.
- ↑ Smith SS, Kaplan BE, Sowers LC, Newman EM (1992). "Mechanism of human methyl-directed DNA methyltransferase and the fidelity of cytosine methylation". Proceedings of the National Academy of Sciences of the United States of America 89 (10): 4748–4744. PMC 49160. PMID 1584813. doi:10.1073/pnas.89.10.4744.
- ↑ Jair KW, Bachman KE, Suzuki H, Ting AH, Rhee I, Yen RW, Baylin SB, Schuebel KE (2006). "De novo CpG Island Methylation in Human Cancer Cells". Cancer Research 69 (2): 682–692. PMID 16423997. doi:10.1158/0008-5472.CAN-05-1980.
- ↑ Ting AH, Jair KW, Schuebel KE, Baylin SB (2006). "Differential Requirement for DNA Methyltransferse 1 In Maintianing Cancer Cell Gene Promoter Hypermethylation". Cancer Research 66 (2): 729–735. PMID 16424002. doi:10.1158/0008-5472.CAN-05-1537.
- ↑ Li E, Bestor TH, Jaenisch R (1992). "Targeted Mutation of the DNA Methyltransferase Gene Results in Embryonic Lethality". Cell 69 (6): 915–926. PMID 1606615. doi:10.1016/0092-8674(92)90611-F.
- ↑ Goll MG, Kirpekar F, Maggert KA, Yoder JA, Hsieh CL, Zhang X, Golic KG, Jacobsen SE, Bestor TH (2006). "Methylation of tRNAAsp by the DNA Methyltransferase Homolog Dnmt2". Science 311 (5759): 395–398. PMID 16424344. doi:10.1126/science.1120976.
- ↑ "TRDMT1 tRNA aspartic acid methyltransferase 1 (Homo sapiens)". Entrez Gene. NCBI. 2010-11-01. Consultado o 2010-11-07.
- ↑ Chédin F. The DNMT3 family of mammalian de novo DNA methyltransferases. Prog Mol Biol Transl Sci. 2011;101:255-85. doi: 10.1016/B978-0-12-387685-0.00007-X. PMID 21507354
- ↑ Mack GS (2010). "To selectivity and beyond". Nat. Biotechnol. 28 (12): 1259–66. PMID 21139608. doi:10.1038/nbt.1724.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]- Metiltransferase
- Metilación do ADN
- Vía PRMT4
Bibliografía
[editar | editar a fonte]- Smith SS (1994). "Biological implications of the mechanism of action of human DNA (cytosine-5)methyltransferase". Prog. Nucleic Acid Res. Mol. Biol. 49: 65–111. PMID 7863011.
- Pradhan S, Esteve PO (2003). "Mammalian DNA (cytosine-5) methyltransferases and their expression". Clin. Immunol. 109 (1): 6–16. PMID 14585271. doi:10.1016/S1521-6616(03)00204-3.
- Goll MG, Bestor TH (2005). "Eukaryotic cytosine methyltransferases". Annu. Rev. Biochem. 74: 481–514. PMID 15952895. doi:10.1146/annurev.biochem.74.010904.153721.
- Svedruzić ZM (2008). "Mammalian cytosine DNA methyltransferase Dnmt1: enzymatic mechanism, novel mechanism-based inhibitors, and RNA-directed DNA methylation". Curr. Med. Chem. 15 (1): 92–106. PMID 18220765. doi:10.2174/092986708783330700.
Ligazóns externas
[editar | editar a fonte]- Información sobre ADN metiltransferases e metilación do ADN en epigeneticstation.com
- Datos para un anticorpo para a ADN metiltransferase (DNMT) Antibody
- DNA Modification Methyltransferases Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
Este artigo contén información en dominio público procedente de Pfam e InterPro IPR001525, IPR003356, IPR012327 e IPR002941.