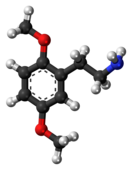
| 2,5-диметоксифенилэтиламин | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
2-(2,5-диметоксифенил)этиламин | ||
| Сокращения | 2C-H | ||
| Хим. формула | C10H15NO2 | ||
| Физические свойства | |||
| Молярная масса | 181,23 г/моль | ||
| Плотность | 1,089 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 139 °C | ||
| Давление пара | 10 (160°C) мм рт.ст. | ||
| Классификация | |||
| Рег. номер CAS | 3600-86-0 | ||
| PubChem | 76632 | ||
| Рег. номер EINECS | 625-021-8 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 125507 | ||
| ChemSpider | 69096 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
2С-Н, или 2,5-диметоксифенилэтиламин — замещённый фенэтиламин из 2C-семьи. 2С-H был впервые синтезирован в 1932 году Йоханнессом С. Баком[1]. В книге PiHKAL не указываются дозировка и длительность эффекта 2С-H. Данных об испытаниях 2С-Н на людях не опубликовано, так как он, вероятно, уничтожается моноаминоксидазой, прежде чем вызывает значительные психотропные эффекты[2]. Существует очень мало данных о фармакологических свойствах, метаболизме и токсичности 2С-Н.
2С-H используется в качестве прекурсора в синтезе других замещённых фенилэтиламинов.
Источники
[править | править код]- ↑ Buck, Johannes S. Hydroxy- and Dihydroxyphenylethylmethylamines and their Ether (неопр.) // Journal of Chemical Society. — 1932. — Т. 54, № 9. — С. 3661—3665. — doi:10.1021/ja01348a024.
- ↑ Alexander Shulgin, Ann Shulgin. 2C-H: Extensions and commentary // PiHKAL: A Chemical Love Story. — Berkeley, California: Transform Press, 1995. — 978 p. — ISBN 0-963-0096-0-5.
Ссылки
[править | править код]- Запись в PubChem
- Запись в NIST WebBook
- [www.erowid.org/library/books_online/pihkal/pihkal032.shtml Информация в PiHKAL]
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист Эти сайты могут нарушать авторские права, быть признаны неавторитетными источниками или по другим причинам быть запрещены в Википедии. Редакторам следует заменить такие ссылки ссылками на соответствующие правилам сайты или библиографическими ссылками на печатные источники либо удалить их (возможно, вместе с подтверждаемым ими содержимым).
.mw-parser-output .ts-Скрытый_блок{margin:0;overflow:hidden;border-collapse:collapse;box-sizing:border-box;font-size:95%}.mw-parser-output .ts-Скрытый_блок-title{text-align:center;font-weight:bold;line-height:1.6em;min-height:1.2em}.mw-parser-output .ts-Скрытый_блок .mw-collapsible-content{overflow-x:auto;overflow-y:hidden;clear:both}.mw-parser-output .ts-Скрытый_блок::before,.mw-parser-output .ts-Скрытый_блок .mw-collapsible-toggle{padding-top:.1em;width:6em;font-weight:normal;font-size:calc(90%/0.95)}.mw-parser-output .ts-Скрытый_блок-rightHideLink .mw-collapsible-toggle{float:right;text-align:right}.mw-parser-output .ts-Скрытый_блок-leftHideLink .mw-collapsible-toggle{float:left;text-align:left}.mw-parser-output .ts-Скрытый_блок-gray{padding:2px;border:1px solid var(--border-color-base,#a2a9b1)}.mw-parser-output .ts-Скрытый_блок-transparent{border:none}.mw-parser-output .ts-Скрытый_блок-gray .ts-Скрытый_блок-title{background:var(--background-color-neutral,#eaecf0);padding:.1em 6em;padding-right:0}.mw-parser-output .ts-Скрытый_блок-transparent .ts-Скрытый_блок-title{background:transparent;padding:.1em 5.5em;padding-right:0}.mw-parser-output .ts-Скрытый_блок-gray .mw-collapsible-content{padding:.25em 1em}.mw-parser-output .ts-Скрытый_блок-transparent .mw-collapsible-content{padding:.25em 0}.mw-parser-output .ts-Скрытый_блок-gray.ts-Скрытый_блок-rightHideLink .mw-collapsible-toggle{padding-right:1em}.mw-parser-output .ts-Скрытый_блок-transparent.ts-Скрытый_блок-rightHideLink .mw-collapsible-toggle{padding-right:0}.mw-parser-output .ts-Скрытый_блок-gray.ts-Скрытый_блок-leftHideLink .mw-collapsible-toggle{padding-left:1em}.mw-parser-output .ts-Скрытый_блок-transparent.ts-Скрытый_блок-leftHideLink .mw-collapsible-toggle{padding-left:0}.mw-parser-output .ts-Скрытый_блок-gray.ts-Скрытый_блок-rightHideLink .ts-Скрытый_блок-title-leftTitle{padding-left:1em}.mw-parser-output .ts-Скрытый_блок-gray.ts-Скрытый_блок-leftHideLink .ts-Скрытый_блок-title-leftTitle{padding-left:6.5em}.mw-parser-output .ts-Скрытый_блок-gray.ts-Скрытый_блок-leftHideLink .ts-Скрытый_блок-title-rightTitle{padding-right:1em}.mw-parser-output .ts-Скрытый_блок-transparent.ts-Скрытый_блок-rightHideLink .ts-Скрытый_блок-title-rightTitle,.mw-parser-output .ts-Скрытый_блок-transparent.ts-Скрытый_блок-rightHideLink .ts-Скрытый_блок-title-leftTitle{padding-left:0}.mw-parser-output .ts-Скрытый_блок-transparent.ts-Скрытый_блок-leftHideLink .ts-Скрытый_блок-title-rightTitle,.mw-parser-output .ts-Скрытый_блок-transparent.ts-Скрытый_блок-leftHideLink .ts-Скрытый_блок-title-leftTitle{padding-right:0}.mw-parser-output .ts-Скрытый_блок+.ts-Скрытый_блок,.mw-parser-output .ts-Скрытый_блок+link+.ts-Скрытый_блок{border-top-style:hidden}Список проблемных ссылок
www.erowid.org/library/books_online/pihkal/pihkal032.shtml