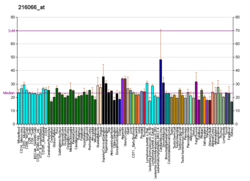
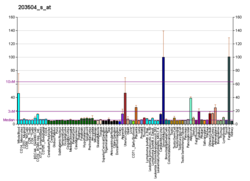
Transporter ABCA1 ATP-vezujuće kasete (član 1 potporodice ljudskih transportera ABCA), poznat i kao regulatorni protein otpuštanja holesterola (CERP) je protein koji je kod ljudi kodiran genom ABCA1.[5] Ovaj transporter je glavni regulator ćelijskog holesterola i homeostaze fosfolipida.
Tangerova bolest
[uredi | uredi izvor]Otkriveno je, u nekoliko grupa, 1998., da je mutacija proteina ABCA1 odgovorna za izazivanje Tangierove bolesti. Grupa Gerda Schmitza u Njemačkoj[6] grupa Michaela Haydena u Britanskoj Kolumbiji [7] koristili su standardne genetičke tehnike i DNK iz porodičnih rodoslova kako bi locirali mutaciju. Grupa Richarda Lawna iz CV Therapeutics-a u Palo Altu, Kalifornija, koristila je cDNK mikrosekvence, koje su u to vrijeme bili relativno nove, za procjenu profila ekspresije gena iz ćelijskih linija stvorenih od normalnih i pogođenih osoba.[8] Pokazali su da su ćelijske linije pacijenata s Tangierovom bolešću imaale diferenciranu regulaciju gena ABCA1. Naknadnim sekvenciranjem gena identificirane su mutacije. Za ovo otkriće, grupa dobila nagradu Američkog udruženja za srce.[9] Tangierova bolest identificirana je kod gotovo 100 pacijenata širom svijeta, koji su imali širok spektar biohemijskih i kliničkih fenotipova jer je identificirano preko 100 različitih mutacija u ABCA1 što je rezultiralo bolešću.[10]
Funkcija
[uredi | uredi izvor]Protein povezan sa membranom, koji je kodiran ovim genom, član je natporodice transportera ATP-vezujuće kasete (ABC). ABC proteini prenose različite molekule kroz vanćelijske i unutarćelijske membrane. ABC geni podijeljeni su u sedam različitih potporodica (ABCA, MDR / TAP, MRP, ALD, OABP, GCN20, White). Ovaj protein je član potporodice ABCA. Njeni članovi čine jedinu glavnu potporodicu ABC koja se nalazi isključivo u višećelijskim eukariotima. Sa holesterolom kao supstratom, ovaj protein funkcionira kao izlivna holesterolska pumpa u ćelijskomom putu uklanjanja lipida.[11][12]
Iako kompletna 3D-struktura ABCA1 ostaje relativno nepoznata, postojala su izvjesna određenja C-kraja. C-kraj ABCA1 sadrži PDZ domen, odgovoran za posredovanje interakcija proteina i proteina, kao i motiv VFVNFA, bitan za aktivnost izliva lipida.[10]
Fiziološka uloga
[uredi | uredi izvor]ABCA1 posreduje izlivu holesterola i fosfolipida u lipidno siromašne apolipoproteine (apoA1 i apoE) (obrnuti transport holesterola), koji zatim formiraju novonastali lipid visoke gustoće (HDL). Također posreduje u transportu lipida između Golgijevog aparata i ćelijske membrane. Budući da je ovaj protein potreban u cijelom tijelu, ispoljava se posvuda i pojavljuje kao protein od 220 kDa. Prisutan je u većim količinama u transportnim tkivima ili onim koja su uključena u promet lipida kao što su jetra, tanko crijevo i masno tkivo.[13]
Faktori koji djeluju na ekspresiju ABCA1 transportera ili njegovu posttranslacijsku modifikaciju također su molekule koje su uključene u njegovu naknadnu funkciju poput masnih kiselina, holesterola, a također i citokina i cAMP-a.[14] Adiponektin inducira reverzni transport holesterola, ovisnim putem o ABCA1.[15] Izvešteno je i da drugi endogeni metaboliti koji su slabije povezani sa funkcijama ABCA1 utiču na ekspresiju ovog transportera, uključujući glukozu i bilirubin.[16][17]
Interakcije između članova porodice apoliproteina i ABCA1 aktiviraju više signalnih puteva, uključujući puteve JAK-STAT, PKA i PKC.[18]
Izvješteno je da prekomjerna ekspresija ABCA1 izaziva rezistenciju na protivupalni diarilheptanoid antioksidans kurkumin.[19] Smanjivanje regulacije ABCA1 u zastarjelim makrofagima narušava sposobnost ćelije da uklanja holesterol iz citoplazme, što dovodi do podsticanja patoloških zadebljanja/otvrdnjavanja krvnih sudova, koje imaju centralnu ulogu u uobičajenim starosnim bolestima poput ateroskleroze, raka i makulske degeneracije.[20] Modeli nokaut-mišje AMD tretirani agonistima koji povećavaju ABCA1 u gubitku funkcije i dobicima od eksperimenata funkcije, pokazali su zaštitnu ulogu podizanja ABCA1 u regulaciji angiogeneze kod očnih bolesti. Podaci ljudima-pacijentima i kontroli korišteni su za demonstraciju analogije nalaza kod miša na ljudsku bolest.
Klinički značaj
[uredi | uredi izvor]Mutacije u ovom genu povezane su sa Tangierovom bolesti i porodičnim nedostatkom lipoproteina velike gustoće. Pokazalo se da je ABCA1 smanjen u Tangierovoj bolesti kod pacijenata koji imaju fiziološke nedostatke HDL-a .[21][22] Ekspresija ABCA1 u leukocitima povećana je kod žena, u postmenopauzi, koje primaju hormonska nadomjesna terapija (HRP).[23]
Interakcije
[uredi | uredi izvor]Pokazalo se da ABCA1 ima interakcija+e sa:
Također pogledajte
[uredi | uredi izvor]- Transporten ATP-vezane kasete
Reference
[uredi | uredi izvor]- ^ a b c GRCh38: Ensembl release 89: ENSG00000165029 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000015243 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Luciani MF, Denizot F, Savary S, Mattei MG, Chimini G (maj 1994). "Cloning of two novel ABC transporters mapping on human chromosome 9". Genomics. 21 (1): 150–9. doi:10.1006/geno.1994.1237. PMID 8088782.
- ^ Bodzioch M, Orsó E, Klucken J, Langmann T, Böttcher A, Diederich W, Drobnik W, Barlage S, Büchler C, Porsch-Ozcürümez M, Kaminski WE, Hahmann HW, Oette K, Rothe G, Aslanidis C, Lackner KJ, Schmitz G (august 1999). "The gene encoding ATP-binding cassette transporter 1 is mutated in Tangier disease". Nature Genetics. 22 (4): 347–51. doi:10.1038/11914. PMID 10431237.
- ^ Brooks-Wilson A, Marcil M, Clee SM, Zhang LH, Roomp K, van Dam M, Yu L, Brewer C, Collins JA, Molhuizen HO, Loubser O, Ouelette BF, Fichter K, Ashbourne-Excoffon KJ, Sensen CW, Scherer S, Mott S, Denis M, Martindale D, Frohlich J, Morgan K, Koop B, Pimstone S, Kastelein JJ, Genest J, Hayden MR (august 1999). "Mutations in ABC1 in Tangier disease and familial high-density lipoprotein deficiency". Nature Genetics. 22 (4): 336–45. doi:10.1038/11905. PMID 10431236.
- ^ Lawn RM, Wade DP, Garvin MR, Wang X, Schwartz K, Porter JG, Seilhamer JJ, Vaughan AM, Oram JF (oktobar 1999). "The Tangier disease gene product ABC1 controls the cellular apolipoprotein-mediated lipid removal pathway". The Journal of Clinical Investigation. 104 (8): R25-31. doi:10.1172/JCI8119. PMC 481052. PMID 10525055.
- ^ "American Heart Association Selects CV Therapeutics' Discovery of Role Of 'Good' Cholesterol-Regulating Gene as Top Ten 1999 Research Advances In Heart Disease" (Press release). CV Therapeutics; Incyte Pharmaceuticals. 3. 1. 2000. Pristupljeno 28. 5. 2018.
- ^ a b Brunham LR, Singaraja RR, Hayden MR (2006). "Variations on a gene: rare and common variants in ABCA1 and their impact on HDL cholesterol levels and atherosclerosis". Annual Review of Nutrition. 26: 105–29. doi:10.1146/annurev.nutr.26.061505.111214. PMID 16704350.
- ^ "Entrez Gene: ABCA1 ATP-binding cassette, sub-family A (ABC1), member 1".
- ^ Schmitz G, Langmann T (april 2001). "Structure, function and regulation of the ABC1 gene product". Current Opinion in Lipidology. 12 (2): 129–40. doi:10.1097/00041433-200104000-00006. PMID 11264984.
- ^ Wagner E, Basso F, Kim CS, Amar MJ (2014). "ABC lipid transporters". AccessScience. McGraw-Hill Education. doi:10.1036/1097-8542.801530.
- ^ Yokoyama S (februar 2006). "ABCA1 and biogenesis of HDL". Journal of Atherosclerosis and Thrombosis. 13 (1): 1–15. doi:10.5551/jat.13.1. PMID 16505586.
- ^ Hafiane A, Gasbarrino K, Daskalopoulou SS (2019). "The role of adiponectin in cholesterol efflux and HDL biogenesis and metabolism". Metabolism: Clinical and Experimental. 100: 153953. doi:10.1016/j.metabol.2019.153953. PMID 31377319.
- ^ Mauerer R, Ebert S, Langmann T (februar 2009). "High glucose, unsaturated and saturated fatty acids differentially regulate expression of ATP-binding cassette transporters ABCA1 and ABCG1 in human macrophages". Experimental & Molecular Medicine. 41 (2): 126–32. doi:10.3858/emm.2009.41.2.015. PMC 2679329. PMID 19287193.
- ^ Wang D, Tosevska A, Heiß EH, Ladurner A, Mölzer C, Wallner M, Bulmer A, Wagner KH, Dirsch VM, Atanasov AG (april 2017). "Bilirubin Decreases Macrophage Cholesterol Efflux and ATP-Binding Cassette Transporter A1 Protein Expression". Journal of the American Heart Association. 6 (5): e005520. doi:10.1161/JAHA.117.005520. PMC 5524097. PMID 28455345.
- ^ Luu W, Sharpe LJ, Gelissen IC, Brown AJ (august 2013). "The role of signalling in cellular cholesterol homeostasis". IUBMB Life. 65 (8): 675–84. doi:10.1002/iub.1182. PMID 23847008.
- ^ Bachmeier BE, Iancu CM, Killian PH, Kronski E, Mirisola V, Angelini G, Jochum M, Nerlich AG, Pfeffer U (decembar 2009). "Overexpression of the ATP binding cassette gene ABCA1 determines resistance to Curcumin in M14 melanoma cells". Molecular Cancer. 8: 129. doi:10.1186/1476-4598-8-129. PMC 2804606. PMID 20030852.
- ^ Sene A, Khan AA, Cox D, Nakamura RE, Santeford A, Kim BM, Sidhu R, Onken MD, Harbour JW, Hagbi-Levi S, Chowers I, Edwards PA, Baldan A, Parks JS, Ory DS, Apte RS (april 2013). "Impaired cholesterol efflux in senescent macrophages promotes age-related macular degeneration". Cell Metabolism. 17 (4): 549–61. doi:10.1016/j.cmet.2013.03.009. PMC 3640261. PMID 23562078.
- ^ Ordovas JM (mart 2000). "ABC1: the gene for Tangier disease and beyond". Nutrition Reviews. 58 (3 Pt 1): 76–9. doi:10.1111/j.1753-4887.2000.tb01843.x. PMID 10812922.
- ^ Oram JF, Vaughan AM (juni 2000). "ABCA1-mediated transport of cellular cholesterol and phospholipids to HDL apolipoproteins". Current Opinion in Lipidology. 11 (3): 253–60. doi:10.1097/00041433-200006000-00005. PMID 10882340.
- ^ Darabi M, Rabbani M, Ani M, Zarean E, Panjehpour M, Movahedian A (septembar 2011). "Increased leukocyte ABCA1 gene expression in post-menopausal women on hormone replacement therapy". Gynecological Endocrinology. 27 (9): 701–5. doi:10.3109/09513590.2010.507826. PMID 20807164.
- ^ Fitzgerald ML, Morris AL, Rhee JS, Andersson LP, Mendez AJ, Freeman MW (septembar 2002). "Naturally occurring mutations in the largest extracellular loops of ABCA1 can disrupt its direct interaction with apolipoprotein A-I". The Journal of Biological Chemistry. 277 (36): 33178–87. doi:10.1074/jbc.M204996200. PMID 12084722.
- ^ Buechler C, Bared SM, Aslanidis C, Ritter M, Drobnik W, Schmitz G (novembar 2002). "Molecular and functional interaction of the ATP-binding cassette transporter A1 with Fas-associated death domain protein". The Journal of Biological Chemistry. 277 (44): 41307–10. doi:10.1074/jbc.C200436200. PMID 12235128.
- ^ Buechler C, Boettcher A, Bared SM, Probst MC, Schmitz G (maj 2002). "The carboxyterminus of the ATP-binding cassette transporter A1 interacts with a beta2-syntrophin/utrophin complex". Biochemical and Biophysical Research Communications. 293 (2): 759–65. doi:10.1016/S0006-291X(02)00303-0. PMID 12054535.
- ^ Shimizu Y, Iwai S, Hanaoka F, Sugasawa K (januar 2003). "Xeroderma pigmentosum group C protein interacts physically and functionally with thymine DNA glycosylase". The EMBO Journal. 22 (1): 164–73. doi:10.1093/emboj/cdg016. PMC 140069. PMID 12505994.
Dopunska literatura
[uredi | uredi izvor]- Tam SP, Mok L, Chimini G, Vasa M, Deeley RG (septembar 2006). "ABCA1 mediates high-affinity uptake of 25-hydroxycholesterol by membrane vesicles and rapid efflux of oxysterol by intact cells". American Journal of Physiology. Cell Physiology. 291 (3): C490-502. doi:10.1152/ajpcell.00055.2006. PMID 16611739.
- Oram JF (august 2002). "ATP-binding cassette transporter A1 and cholesterol trafficking". Current Opinion in Lipidology. 13 (4): 373–81. doi:10.1097/00041433-200208000-00004. PMID 12151852.
- Hong SH, Rhyne J, Zeller K, Miller M (oktobar 2002). "ABCA1(Alabama): a novel variant associated with HDL deficiency and premature coronary artery disease". Atherosclerosis. 164 (2): 245–50. doi:10.1016/S0021-9150(02)00106-5. PMID 12204794.
- Kozak M (august 2002). "Emerging links between initiation of translation and human diseases". Mammalian Genome. 13 (8): 401–10. doi:10.1007/s00335-002-4002-5. PMID 12226704.
- Joyce C, Freeman L, Brewer HB, Santamarina-Fojo S (juni 2003). "Study of ABCA1 function in transgenic mice". Arteriosclerosis, Thrombosis, and Vascular Biology. 23 (6): 965–71. doi:10.1161/01.ATV.0000055194.85073.FF. PMID 12615681.
- Singaraja RR, Brunham LR, Visscher H, Kastelein JJ, Hayden MR (august 2003). "Efflux and atherosclerosis: the clinical and biochemical impact of variations in the ABCA1 gene". Arteriosclerosis, Thrombosis, and Vascular Biology. 23 (8): 1322–32. doi:10.1161/01.ATV.0000078520.89539.77. PMID 12763760.
- Nofer JR, Remaley AT (oktobar 2005). "Tangier disease: still more questions than answers". Cellular and Molecular Life Sciences. 62 (19–20): 2150–60. doi:10.1007/s00018-005-5125-0. PMID 16235041.
- Yokoyama S (februar 2006). "ABCA1 and biogenesis of HDL". Journal of Atherosclerosis and Thrombosis. 13 (1): 1–15. doi:10.5551/jat.13.1. PMID 16505586.
- Schmitz G, Schambeck CM (2006). "Molecular defects in the ABCA1 pathway affect platelet function". Pathophysiology of Haemostasis and Thrombosis. 35 (1–2): 166–74. doi:10.1159/000093563. PMID 16855366.
Vanjski linkovi
[uredi | uredi izvor]- ABCA1 lokacija ljudskog genoma UCSC Genome Browser.
ABCA1 detalji ljudskog genoma u UCSC Genome Browser.
| A | |
|---|---|
| B |
|
| C |
|
| D |
|
| E |
|
| F |
|
| G | |
Također pogledajte Poremećaji ABC transportera | |
Šablon:Lipoproteini