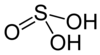
Kwas siarkawy, nazwa Stocka: kwas siarkowy(IV), H
2SO
3 – nieorganiczny związek chemiczny nietrwały kwas tlenowy o słabej/średniej mocy[6][7][8].
Występowanie i właściwości
Jest nieznany w stanie czystym i określany bywa także jako wodny roztwór dwutlenku siarki[1][2][9], jednak w roztworze takim występują liczne indywidua chemiczne, głównie różne hydraty SO
2·nH
2O, a także jony H
3O+
, HSO−
3, S
2O2−
5 i śladowe ilości SO2−
3. W roztworze nie wykryto natomiast cząsteczek H
2SO
3 i przyjmuje się, że jeśli w ogóle one istnieją, to stała równowagi reakcji SO
2·nH
2O ⇌ H
2SO
3 jest znacznie mniejsza od 10−9. Cząsteczki H
2SO
3 wykryto natomiast w fazie gazowej w warunkach jonizacji w spektrometrze masowym[10].
Nasycony roztwór ma stężenie ok. 6%[2] i gęstość 1,03 g/cm³[4].
W temperaturze 0 °C z roztworu wytrącają się hydraty typu klatratów o przybliżonym składzie SO
2·6H
2O[10]. Z metalami tworzy sole – wodorosiarczyny i siarczyny; te drugie są stosunkowo trwałe i wiele z nich otrzymano w formie krystalicznej[10].
Otrzymywanie
Powstawanie kwasu siarkawego:
- SO
2 + H
2O → H
2SO
3
Można go także otrzymać działając roztworem mocnego kwasu na siarczyny. Powstały wówczas kwas siarkawy ulega rozpadowi według równania:
- SO2−
3 + 2H+
→ [H
2SO
3] → SO
2↑ + H
2O
Właściwości
Właściwości kwasu siarkawego:
- nietrwały – rozkłada się podczas ogrzewania,
- bakteriobójczy,
- grzybobójczy,
- ma właściwości bielące,
- niszczy rośliny,
- trujący,
- silnie drażniący,
- jest elektrolitem.
W przeciwieństwie do swoich soli, siarczynów, zastosowanie wolnego kwasu siarkawego jest znikome. W syntezie laboratoryjnej wykorzystuje się go jako środek redukujący. Stosuje się go do bielenia wełny oraz w przemyśle papierniczym.
Kwaśny deszcz to silnie rozcieńczony kwas siarkawy, który powstaje w wyniku rozpuszczania się w kroplach deszczu dwutlenku siarki, pochodzącego głównie ze spalania zasiarczonych paliw kopalnianych: węgla, gazu ziemnego oraz paliw ropopochodnych.
W warunkach laboratoryjnych kwas siarkawy można otrzymać poprzez spalanie siarki i absorpcję powstających par w wodzie, w wyniku czego powstaje niezbyt stężony roztwór tego kwasu.