La farmacocinetica è la branca della farmacologia che studia la distribuzione dei farmaci nell'organismo e il loro destino, in relazione alle dosi, alle vie di somministrazione e alle forme farmaceutiche.[1][2] In particolare essa studia, da un punto di vista quantitativo, l'assorbimento, la distribuzione, il metabolismo e l'escrezione (ADME) dei farmaci.[3] La precisa conoscenza dal punto di vista quantitativo e qualitativo di questi processi consente di definire il dosaggio utile di un farmaco rispetto alle diverse condizioni di un soggetto, come l'età, la presenza di particolari patologie e alcune situazioni fisiologiche.[4]
Storia
[modifica | modifica wikitesto]La farmacocinetica nasce tra la fine del XIX sec. e l'inizio del XX sec. quando iniziarono e presero corpo gli studi sull'assorbimento, la biotrasformazione, la distribuzione e l'eliminazione dei farmaci. Già nel XVIII sec. si ipotizzava che non solo i farmaci modificassero l'organismo, ma anche che l'organismo modificasse i farmaci. La conoscenza dei valori farmacocinetici di un medicinale ha condizionato profondamente lo sviluppo di queste sostanze, in particolare ha portato alla realizzazione di specifiche preparazioni farmaceutiche come le forme retard e allo sviluppo di dispositivi che consentono al farmaco di raggiungere distretti dell'organismo altrimenti inaccessibili.
L'acronimo ADME venne presentato per la prima volta da Nelson nel 1961, parafrasando riassorbimento, distribuzione, consumo ed eliminazione utilizzato da Teorell nel 1937.[5][6] Ulteriori studi di rilievo in questa disciplina includono la descrizione dell'eliminazione di primo ordine fatta da Widmark nel 1919 e il trattato di Dost del 1953 dove viene definito il termine farmacocinetica.[7][8]
Inizialmente il termine definiva gli identificatori quantitativi del farmaco che entra nel corpo (A), si muove attraverso il corpo (D), si modifica all'interno del corpo (M) e lascia il corpo (E). Nel corso del tempo l'uso dell'acronimo si è modificato arrivando a descrivere i meccanismi di: attraversamento della parte dello stomaco (A), spostamento attraverso i compartimenti (D), metabolizzazione (M) ed escrezione o eliminazione (E) a cui a volte si aggiunge il trasporto (T).[3]
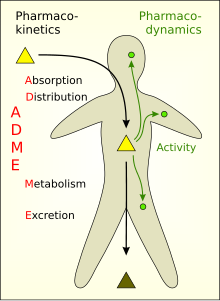
ADME
[modifica | modifica wikitesto]In linea generale la farmacocinetica il percorso del principio attivo del farmaco attraverso il corpo con il passare del tempo.[3] I quattro processi che descrivono il destino del farmaco all'interno dell'organismo sono:[9]
- assorbimento
- distribuzione
- biotrasformazione
- eliminazione
Assorbimento
[modifica | modifica wikitesto]La fase di assorbimento descrive il passaggio del farmaco dalla sede di somministrazione al circolo sistemico.[10]
Vie di somministrazione
[modifica | modifica wikitesto]Il fattore che influenza maggiormente l'assorbimento è la via di somministrazione, ossia il modo che si sceglie per far penetrare il farmaco nell'organismo. Il medico ed il farmacologo scelgono fra le diverse vie di somministrazione a seconda delle caratteristiche chimico-fisiche del farmaco, della velocità con cui vogliono che esso venga assorbito (assorbimento più rapido per le vie parenterali, più lento per quelle enterali) e della velocità con cui vogliono che il farmaco venga metabolizzato ed eliminato.[11]
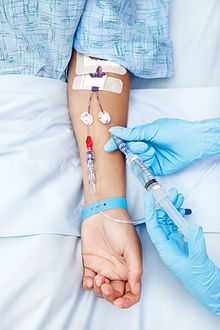


Le vie di somministrazione possono essere classificate in diversi modi; una prima classificazione distingue fra:[11][12]
- vie enterali (orale, sublinguale, buccale, rettale)
- vie parenterali (endovena, intramuscolo, sottocutanea)
Una seconda classificazione distingue:
- vie sistemiche (quando il farmaco agisce su bersagli distanti dalla sede di somministrazione)
- vie topiche (quando il farmaco agisce localmente nella sede di somministrazione)
Infine, una terza classificazione individua:
- vie naturali (quando l'assorbimento avviene attraverso epiteli di cute o mucose)
- vie artificiali (quando la somministrazione necessita dell'uso di presidi medici quali aghi, siringhe ecc)
Alcune tra le più comuni vie di somministrazione sono elencate nella tabella seguente.
| Via di somministrazione | Assorbimento | Forme farmaceutiche | Caratteristiche particolari | |||
|---|---|---|---|---|---|---|
| Sistemica | naturale | Enterale | Orale | Variabile, dipende da molti fattori | Compresse, pastiglie, sciroppi, gocce | La più utilizzata (70%), non necessita di particolari presidi medici |
| Sublinguale | Rapido | Compresse, perle, spray | Evita l'effetto di primo passaggio epatico | |||
| Buccale | Rapido | Compresse o lollipop | L'assorbimento avviene tenendo la compressa tra guancia e gengiva | |||
| Rettale | Rapido | Supposte | Possono essere somministrate anche in pazienti non coscienti o incapaci di collaborare | |||
| Respiratoria | Rapidissimo, per l'ampia superficie alveolare | Gas | ||||
| artificiale | Parenterale | Endovenosa | Nessuno: il farmaco viene immesso direttamente nel circolo sistemico | Boli o fleboclisi | Possono essere somministrate solo soluzioni (mai sospensioni) di sostanze non irritanti (rischio di anafilassi) e non oleose (rischio di embolia lipidica) | |
| Intramuscolare | Condizionato dall'area della superficie assorbente | Boli | Possono essere somministrate anche sostanze oleose; non può essere usata in corso di terapia con anticoagulanti (rischio di emorragia) | |||
| Sottocutanea | Modulabile | Boli, pellets | Possono essere somministrate anche sospensioni, ma non sostanze irritanti (rischio di necrosi cutanea); può essere usata per l'impianto di pellets solidi a lento rilascio | |||
| Topica | naturale | Inalatoria | Va evitato, per scongiurare il pericolo di effetti indesiderati a distanza | Aerosol | Parte del farmaco viene assorbito tramite la superficie bronchiale, un'altra parte invece viene deglutita e assorbita per via orale | |
| Sistemica o topica | naturale | Transdermica | Facilitato se la cute è sottile | Creme, pomate, cerotti a rilascio controllato | Solo per farmaci molto liposolubili | |
Fattori che influenzano l'assorbimento
[modifica | modifica wikitesto]Esistono poi diversi fattori che influenzano l'assorbimento del farmaco e possono essere divisi in:[13][14][15]
- farmaco-specifici
- caratteristiche chimico-fisiche:
- la solubilità del farmaco
- l'effetto del pH e della pKa
- la dimensione delle particelle
- l'area superficiale
- il tasso di dissoluzione
- la disposizione spaziale degli atomi e delle molecole
- la concentrazione del farmaco
- la presenza di eccipienti
- formato
- via di somministrazione
- caratteristiche chimico-fisiche:
- paziente-specifici
- età
- velocità di svuotamento gastrico
- velocità di transito intestinale
- flusso sanguigno nel sito di assorbimento
- area della superficie assorbente
- malattie
- metabolismo
- contenuto del tratto gastrointestinale
Solubilità
[modifica | modifica wikitesto]In base alla solubilità del composto questo verrà assorbito in maniera diversa dall'organismo:[16]
- le sostanze insolubili in acqua vengono assorbite mediante endocitosi
- le sostanze idrosolubili non ionizzabili con superficie polare <4 Å vengono assorbite per filtrazione
- le sostanze idrosolubili non ionizzabili con superficie polare >4 Å e le sostanze ionizzate a pH organici vengono assorbite mediante trasporto mediato da carrier
- le sostanze liposolubili vengono assorbite mediante diffusione
Effetto del pH e della pKa
[modifica | modifica wikitesto]Molti farmaci agiscono come acidi o basi deboli in forma ionizzata e non ionizzata. La distribuzione di elettroliti deboli attraverso la membrana è il risultato del gradiente di pH e della costante di dissociazione acida del medicinale. I medicinali che si comportano come acidi deboli vengono facilmente assorbiti in ambiente acido come quello dello stomaco, mentre i farmaci che si comportano come basi deboli non vengono assorbiti finché non raggiungono l'intestino tenue dove il pH è più alto.[17][18]
Tasso di dissoluzione
[modifica | modifica wikitesto]Il tasso di dissoluzione rappresenta la quantità di sostanza solida con un'area superficiale costante che torna in soluzione in condizioni standard di pH, composizione del solvente e temperatura. La dimensione delle particelle è inveramente proporzionale al tasso di dissoluzione, pertanto riducendo la dimensione delle particelle si aumenta il tasso di dissoluzione e viceversa.
Meccanismi di assorbimento
[modifica | modifica wikitesto]Sono stati identificati diversi meccanismi di assorbimento dei farmaci, inclusi la diffusione passiva, il trasporto transmembrana mediato da carrier (diffusione attiva e diffusione facilitata) e altri trasportatori aspecifici come la P-glicoproteina.[16]
Diffusione passiva
[modifica | modifica wikitesto]La diffusione passiva è il meccanismo d'assorbimento più comune e può essere spiegato utilizzando le leggi di Fick secondo cui le molecole del farmaco si spostano secondo il gradiente di concentrazione da quella più alta a quella più bassa fino al raggiungimento dell'equilibrio.[19] Essa può verificarsi sia in ambiente acquoso (spazio interstiziale o pori nell'endotelio dei vasi sanguigni) che in ambiente lipidico. Il coefficiente di ripartizione del farmaco tra le due fasi può dunque essere utilizzato per stabilire quanto velocemente il medicinale si sposti tra di esse.[16]
Trasporto transmembrana mediato da carrier
[modifica | modifica wikitesto]
Il secondo meccanismo di assorbimento più comune è il trasporto transmembrana mediato da carrier. Nel corpo sono presenti numerosi sistemi di trasporto transmembrana mediati da carrier per il trasporto di ioni e nutrienti, specialmente nell'intestino. Questi includono:[16]
- la diffusione attiva
- la diffusione facilitata
Diffusione attiva
[modifica | modifica wikitesto]Si tratta di un sistema che consuma energia ed è essenziale per l'assorbimento dei medicinali nell'apparato gastrointestinale ovvero per la loro escrezione per via renale e biliare. Essa permette il trasporto contro gradiente. Il medicinale si lega al carrier formando un complesso che facilita il trasporto del composto attraverso la membrana per poi dissociarsi. La molecola carrier può essere altamente specifica e farmaci con con strutture simili possono competere per legarsi al carrier nei siti d'assorbimento. Dato il numero ridotto di carrier nel sito d'assorbimento questo può saturarsi velocemente qualora la concentrazione del farmaco sia molto elevata arrivando dunque a renderlo inefficace.[16] Mentre alcuni carrier facilitano il trasporto altri possono invece l'effetto opposto, come nel caso della P-glicoproteina che facilita la secrezione di molecole nel lume intestinale riducendo l'assorbimento dei farmaci.[20]
Diffusione facilitata
[modifica | modifica wikitesto]La diffusione facilitata gioca un ruolo minore nell'assorbimento. Per molti versi simile alla diffusione attiva (sottoposta a saturazione, selettività e cinetica competitiva), la diffusione facilitata differisce da quest'ultima poiché non richiede l'utilizzo di energia e non permette il trasporto contro gradiente.[16] Un esempio di questo sistema è polipeptide trasportatore di cationi organici 1 (OCT1) che facilita l'assorbimento di farmaci come la metformina.[21]
Distribuzione
[modifica | modifica wikitesto]La distribuzione è la seconda fase della farmacocinetica ed esprime il passaggio del farmaco dal circolo sistemico ai tessuti periferici. Anche la distribuzione è influenzata da diversi fattori.
- Grado di liposolubilità del farmaco: condiziona il suo volume di distribuzione.
- Permeabilità dei capillari: condiziona l'extravasazione delle sostanze non liposolubili, che è maggiore nei distretti provvisti di capillari fenestrati (fegato, milza, midollo osseo) piuttosto che in quelle zone dotate di una circolazione altamente impermeabile (barriera ematoencefalica).
- Flusso ematico ai diversi organi: siccome alcuni organi (rene, cuore, fegato) sono maggiormente vascolarizzati di altri (connettivi, adipe), questi ultimi riceveranno il farmaco più tardi degli altri.
- Legame alle proteine plasmatiche: alcune sostanze molto liposolubili non riescono a stare a contatto con l'ambiente acquoso del plasma, pertanto si legano a particolari "tasche" idrofobiche di alcune proteine plasmatiche, come l'albumina, dalle quali fuoriescono solo molto lentamente.
Biotrasformazione
[modifica | modifica wikitesto]La biotrasformazione descrive il metabolismo del farmaco ad opera di specifici enzimi, detti appunto "farmacometabolici". Questi enzimi si trovano in diversi distretti corporei, tra cui fegato (soprattutto), intestino, reni, polmoni, cute, plasma e sistema nervoso centrale, ed hanno in linea di massima lo scopo di trasformare i farmaci in molecole maggiormente solubili, e quindi più facili da eliminare attraverso le urine (con l'eccezione delle reazioni di acetilazione e metilazione).
Le reazioni di biotrasformazione si dividono in due grandi gruppi:
- Reazioni di fase I o "non sintetiche": si compongono di reazioni di ossidoriduzione e di idrolisi; le prime avvengono principalmente nel reticolo endoplasmatico liscio degli epatociti, ad opera di enzimi particolari chiamati citocromi.
- Reazione di fase II o "sintetiche": sono reazioni di coniugazione, mediate da diversi enzimi e cofattori, che aggiungono diversi gruppi funzionali al farmaco allo scopo di renderlo più facilmente eliminabile; le principali reazioni di fase II sono la coniugazione con acido glucuronico (o glicuronoconiugazione), l'acetilazione, la coniugazione con amminoacidi (soprattutto glicina, taurina e glutammina), la coniugazione con solfato (o solfoconiugazione) e la metilazione.
Eliminazione
[modifica | modifica wikitesto]L'eliminazione è la quarta ed ultima fase della farmacocinetica, e descrive tutti quei processi mirati all'escrezione del farmaco, o del suo metabolita, dall'organismo.
Le possibili vie di eliminazione si dividono in:
- Principali: espressamente costituite a questo scopo, sono costituite a loro volta dalle vie:
- renale: è quella maggiormente utilizzata, ma solo per le sostanze idrosolubili, che vengono filtrate dai capillari glomerulari ed eliminati con le urine;
- epatica: alcuni metaboliti non idrosolubili vengono direttamente immessi nel circolo biliare, da cui giungono nell'intestino e vengono eliminati con le feci;
- polmonare: solo per le sostanze volatili, anche se non sono state assorbite per via inalatoria (es. etanolo).
- Accessorie: secrezioni ghiandolari nelle quali accidentalmente possono riversarsi i farmaci, costituite da:
- saliva: in linea di massima il farmaco viene deglutito e riassorbito per via orale;
- sudore;
- lacrime;
- latte.
Interazioni tra farmaci
[modifica | modifica wikitesto]Nel 2023 il MIT ha sviluppato un modello per studiare le interazioni tra farmaci attraverso l'analisi delle loro proteine trasportatrici del tratto gastrointestinale all'interno di un tratto di intestino di maiale coltivato in laboratorio.[22]
Note
[modifica | modifica wikitesto]- ^ Farmacocinetica: definizione e significato medico | Corriere Salute, su www.corriere.it. URL consultato l'8 luglio 2024.
- ^ M. Nordberg, J. Duffus e D. M. Templeton, Glossary of terms used in toxicokinetics (IUPAC Recommendations 2003), in Pure and Applied Chemistry, vol. 76, n. 5, 1º gennaio 2004, pp. 1033–1082, DOI:10.1351/pac200476051033. URL consultato l'8 luglio 2024.
- ^ a b c Matthew P. Doogue e Thomas M. Polasek, The ABCD of clinical pharmacokinetics, in Therapeutic Advances in Drug Safety, vol. 4, n. 1, 2013-02, pp. 5–7, DOI:10.1177/2042098612469335. URL consultato l'8 luglio 2024.
- ^ Luciano Caprino, Il farmaco, 7000 anni di storia. Dal rimedio empirico alle biotecnologie. (PDF), Roma, Armando Editore, AIFA, 2011, p. 15, ISBN 9788866770145.
- ^ Eino Nelson, Kinetics of Drug Absorption, Distribution, Metabolism, and Excretion, in Journal of Pharmaceutical Sciences, vol. 50, n. 3, 1961-03, pp. 181–192, DOI:10.1002/jps.2600500302. URL consultato l'8 luglio 2024.
- ^ Torsten Teorell, STUDIES ON THE DIFFUSION EFFECT UPON IONIC DISTRIBUTION, in Journal of General Physiology, vol. 21, n. 1, 20 settembre 1937, pp. 107–122, DOI:10.1085/jgp.21.1.107. URL consultato l'8 luglio 2024.
- ^ ERIK M. P. WIDMARK, Studies in the concentration of indifferent narcotics in blood and tissues, in Acta Medica Scandinavica, vol. 52, n. 1, 12 gennaio 1919, pp. 87–164, DOI:10.1111/j.0954-6820.1919.tb08277.x. URL consultato l'8 luglio 2024.
- ^ Dost F., Der Blutspiegel: Kinetic der Konzentrationsablaufe in der Krieslaujflussigkeit., Lipsia, Thieme, (1953).
- ^ (EN) Open Resources for Nursing (Open Rn), 1.2 Pharmacokinetics, 2020. URL consultato l'8 luglio 2024.
- ^ Geoffrey M. Currie, Pharmacology, Part 2: Introduction to Pharmacokinetics, in Journal of Nuclear Medicine Technology, vol. 46, n. 3, 3 maggio 2018, pp. 221–230, DOI:10.2967/jnmt.117.199638. URL consultato l'8 luglio 2024.
- ^ a b (EN) Kim J e De Jesus O, Medication Routes of Administration, in StatPearls, Treasure Island (FL), StatPearls Publishing, 23 agosto 2023.
- ^ Le vie di somministrazione (PDF), su infermieristica.polodidatticopanico.com.
- ^ PRINCIPI DI FARMACOCINETICA (PDF), su elearning.unipd.it.
- ^ Farmacologia generale (PDF), su moodle2.units.it.
- ^ Helen Spleis, Matthias Sandmeier e Victor Claus, Surface design of nanocarriers: Key to more efficient oral drug delivery systems, in Advances in Colloid and Interface Science, vol. 313, 2023-03, pp. 102848, DOI:10.1016/j.cis.2023.102848. URL consultato l'8 luglio 2024.
- ^ a b c d e f (EN) Alagga AA, Pellegrini MV e Gupta V, Drug Absorption., in StatPearls Publishing, Treasure Island (FL), 27 febbraio 2024. URL consultato l'8 luglio 2024.
- ^ Marilyn N. Martinez e Gordon L. Amidon, A Mechanistic Approach to Understanding the Factors Affecting Drug Absorption: A Review of Fundamentals, in The Journal of Clinical Pharmacology, vol. 42, n. 6, 2002-06, pp. 620–643, DOI:10.1177/00970002042006005. URL consultato l'8 luglio 2024.
- ^ Laura Stoll e Lisa Gentile, Linking tricyclic antidepressants to ionotropic glutamate receptors, in Biochemical and Biophysical Research Communications, vol. 333, n. 2, 2005-07, pp. 622–627, DOI:10.1016/j.bbrc.2005.05.114. URL consultato l'8 luglio 2024.
- ^ Clément Bielinski e Badr Kaoui, Numerical method to characterise capsule membrane permeability for controlled drug delivery, in International Journal for Numerical Methods in Biomedical Engineering, vol. 38, n. 2, 23 novembre 2021, DOI:10.1002/cnm.3551. URL consultato l'8 luglio 2024.
- ^ Hiroki Sunakawa, Kenta Mizoi e Reiko Takahashi, Impact of P-Glycoprotein-Mediated Drug-Endogenous Substrate Interactions on Androgen and Blood-Brain Barrier Permeability, in Journal of Pharmaceutical Sciences, vol. 113, n. 1, 2024-01, pp. 228–234, DOI:10.1016/j.xphs.2023.10.034. URL consultato l'8 luglio 2024.
- ^ T. Dujic, A. Causevic e T. Bego, Organic cation transporter 1 variants and gastrointestinal side effects of metformin in patients with Type 2 diabetes, in Diabetic Medicine, vol. 33, n. 4, 24 dicembre 2015, pp. 511–514, DOI:10.1111/dme.13040. URL consultato l'8 luglio 2024.
- ^ Interazioni tra farmaci, nuovo modello svela quali non somministrare insieme | Farmacista33, su www.farmacista33.it. URL consultato il 1º marzo 2024.
Bibliografia
[modifica | modifica wikitesto]- Aldo Rescigno, Foundations of Pharmacokinetics, New York, Kluwer Academic/Plenum Publishers, 2003.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikizionario contiene il lemma di dizionario «farmacocinetica»
Wikizionario contiene il lemma di dizionario «farmacocinetica» Wikimedia Commons contiene immagini o altri file sulla farmacocinetica
Wikimedia Commons contiene immagini o altri file sulla farmacocinetica
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) IUPAC Gold Book, "pharmacokinetics", su goldbook.iupac.org.
| Controllo di autorità | LCCN (EN) sh85100597 · GND (DE) 4115557-9 · J9U (EN, HE) 987007541288005171 · NDL (EN, JA) 01033752 |
|---|